Сравнение скорости изменения липидного профиля сыворотки крови человека при подъеме на высоту
Опубликовано в журнале Физиология человека, 2011, том 37, №3. - с. 103-108.
Сравнение скорости изменения липидного профиля сыворотки крови человека при подъеме на высоту среднегорья
Минвалеев Р.С.
Санкт-Петербургский государственный университет
В статье рассматриваются антиатерогенные изменения липидного профиля сыворотки крови в различных условиях: 1) горноклиматическое лечение на курортах кавказского среднегорья, 2) периодическая гипобарическая терапия, 3) треккинг в среднегорье с регулярными холодовыми испытаниями на фоне выполнения специальных упражнений для повышения холодоустойчивости (тибетская йога туммо). Применением экспоненциальной модели выполнено сравнение скоростей изменения общего холестерина, липопротеинов высокой (ЛПВП), низкой (ЛПНП) и очень низкой плотностей (ЛПОНП), а также триглицеридов в сыворотке крови. Применением нового вычислительного алгоритма доказано, что наибольшая скорость антиатерогенных изменений липидного профиля крови (снижение общего холестерина и ЛПНП, повышение ЛПВП) характерна для сочетания высотной гипоксии, умеренных физических нагрузок и выполнения специальных упражнений для повышения холодоустойчивости (тибетская йога туммо).
Ключевые слова: липидный профиль, индекс атерогенности, высотная гипоксия, холодоустойчивость.
Развиты результаты работ [1, 2], в которых мы исследовали липопротеидный профиль сыворотки крови при подъеме на высоту в сочетании с регулярным выполнением специальных упражнений для повышения холодоустойчивости организма человека, историческим аналогом которых является тибетская йога туммо [4].
Согласно содержанию ряда работ [6-18] подъем человека в горы может изменять липидный профиль крови. Интерес исследователей вызывают антиатерогенные изменения липидного профиля (снижение общего холестерина (ХС) и увеличение антиатерогенных липопротеидов высокой плотности (ЛПВП)) при проживании в среднегорье [6, 7], что позволяет использовать горный климат и высотную гипоксию, в том числе для устранения дислипидопротеидемий в профилактике и санаторно-курортном лечении атеросклеротических изменений артериальных сосудов [9, 14-18]. Однако антиатерогенные влияния горного климата и высотной гипоксии на липидный профиль сыворотки крови не подтверждаются в контрольных исследованиях. Австрийские исследователи не обнаружили у 22 мужчин с метаболическим синдромом антиатерогенных изменений липидного профиля после 3 недель пребывания на высоте 1500-2500 м в австрийских Альпах [11]. Более того, накапливаются противоположные данные об увеличении риска атеросклероза сердечно-сосудистой системы при проживании на высоте в связи с увеличением уровня холестерина в крови. Так в работе [12] зафиксировано, что акклиматизация к высоте 3105 мповысила содержание общего холестерина в среднем со 177 до 190 мг/дл (p<0.002) и привела к существенному возрастанию риска атеросклеротической патологии. В недавнем многоцентровом исследовании, проведенном в Швейцарии и опубликованном в 2008 году, на большом числе испытуемых (n = 19272) также не обнаружено значимых изменений содержания холестерина в сыворотке крови при проживании на высоте [13].
Сформулируем противоречие. С одной стороны, подъем и пребывание на высоте применяются как горноклиматическое лечение атеросклероза и немедикаментозная профилактика атерогенных дислипидопротеидемий [1-6, 9-11, 14-18]. С другой стороны, антиатерогенные влияния умеренной высотной гипоксии на липидный состав крови не подтверждается контрольными исследованиями на достаточно больших выборках [8, 12, 13].
По нашему мнению, данное противоречие отражает разную степень гипоксического воздействия на организм человека. Сочетание высотной (пониженное барометрическое давление) и рабочей (дозированная физическая нагрузка) гипоксии характеризует условия, при которых в ряде исследований были найдены антиатерогенные изменения липидного профиля испытуемых (снижение общего холестерина и повышение ЛПВП). Речь идет о различных вариантах спортивного или санаторного режима пребывания в среднегорье и высокогорье [1-6, 9-11, 14-18]. Наоборот, пассивное проживание или подъем на высоту без сопутствующих физических нагрузок могут привести и приводят к противоположным изменениям липидного профиля сыворотки крови здоровых и больных людей [7, 8, 12, 13].
Предполагая, что условиями, определяющими антиатерогенные изменения липидного профиля (снижение общего холестерина и ЛПНП и повышение ЛПВП) при горноклиматическом лечении дислипидопротеидемий, являются сочетание высотной и рабочей гипоксии на фоне регулярных холодовых воздействий (горноклиматическое лечение), мы поставили перед собой задачу сравнения скоростей изменения липидного профиля при различных вариантах изолированного и сочетанного гипоксического и климатического воздействий.
Материалы и методы
Сравнению были подвергнуты результаты измерений липидного профиля, в которых зарегистрировано изменение содержания липидных фракций при пребывании в горах на ограниченном интервале времени (не больше 30 дней). Выбор отечественных работ обусловлен тем, что горноклиматическая коррекция атерогенных дислипидопротеидемий в кардиологии достаточно широко применялась именно в отечественных санаториях, расположенных на курортах среднегорья [14-18].
Из содержания работы [15] мы извлекли численные данные об изменении общего холестерина в процессе лечения на Пятигорском курорте (Таблица 1):
Таблица 1
Содержание общего холестерина в крови в процессе лечения (X±m)
|
Возрастная группа |
Частота благоприятного эффекта (число больных) |
Уровень общего холестерина в крови, ммоль/л |
|
|
в начале курса |
в конце курса |
||
|
1 |
2 |
3 |
4 |
|
41-50 лет |
17 из 18 |
7.77±0.163 |
6.68±0.173 |
|
51-60 лет |
21 из 28 |
7.69±0.158 |
6.63±0.224 |
|
Старше 60 |
13 из 19 |
7.64±0.198 |
6.93±0.186 |
Замечание. В целях удобства для последующего аналитического сравнения скоростей изменения содержания липидов численные данные по первым двум возрастным группам были объединены в одну выборку, для которой суммированы точечные оценки начальных и центральных моментов обеих возрастных групп (согласно содержанию свойств суммы математических ожиданий и дисперсий, а также в силу независимости разбиений по возрастам, такие действия правомерны [19, с. 81, 91]). Вновь вычисленные средневзвешенные (с учетом общего количества обследованных в каждой из двух групп – столбец 2 в таблице 1) значения уровней общего холестерина по объединенной выборке далее были представлены в мг/дл: до лечения (X±m) - 297±11.6 мг/дл, после лечения - 260±13.1 мг/дл.
Из содержания работы [16] мы извлекли численные данные об изменении липидного профиля, которые представлены в таблице 2:
Таблица 2
Содержание липидов в сыворотке крови больных, перенесших крупноочаговый инфаркт миокарда до и после пребывания в условиях среднегорья в течение 30 дней (X±m)
|
Показатель |
До лечения |
Сразу после лечения |
|
1 |
2 |
3 |
|
Общий холестерин (ХС), мг/дл |
241±5.05 |
228±6.51 |
|
Холестерин ЛПВП, мг/дл |
37.5±0.95 |
42.9±1.01* |
|
Триглицериды (ТГ), мг/дл |
215.3±10.3 |
170.8±11.2* |
|
Холестерин ЛПНП, мг/дл |
161.0±6.78 |
155.9±6.51 |
|
Холестерин ЛПОНП, мг/дл |
44.4±2.03 |
35.0±2.51* |
|
Индекс атерогенности (ИА), отн.ед. |
5.42±0.43 |
4.32±0.54 |
Замечание. Несмотря на то, что по ряду показателей изменения недостоверны (достоверные различия с учетом указанного числа испытуемых (n=225) помечены * [16]), в дальнейшем для решения задачи сравнения скоростей изменения липидов будут использованы только средние арифметические найденных характеристик (X).
Из содержания работы [18] мы извлекли численные данные об изменении липидного профиля под воздействием 22-дневной адаптации к периодической барокамерной гипоксии (АПБГ) (Таблица 3):
Таблица 3
Влияние АПБГ на уровень липидов крови больных ИБС (X±m)
|
Показатель |
До АПБГ(1) n=46 |
После АПБГ(2) n=46 |
p1 - 2 |
|
1 |
2 |
3 |
4 |
|
ХС, ммоль/л |
5.29±0.14 |
4.96±0.10 |
<0.002 |
|
ЛПВП, ммоль/л |
1.28±0.05 |
1.36±0.04 |
<0.02 |
|
ЛПОНП, ммоль/л |
0.30±0.018 |
0.26±0.016 |
<0.01 |
|
ЛПНП, ммоль/л |
3.70±0.14 |
3.33±0.11 |
<0.0004 |
|
ТГ, ммоль/л |
1.49±0.09 |
1.29±0.08 |
<0.007 |
|
ИА, отн.ед |
3.56±0.27 |
2.83±0.17 |
<0.0001 |
Замечание. В целях удобства для последующего аналитического сравнения скоростей изменения содержания липидов во второй строке у каждого показателя приведены их численные значения в мг/дл (Коэффициент пересчета численных значений содержания липидов из ммоль/л в мг/дл для холестерина и его фракций в составе липопротеидов принят равным 38.6, для триглицеридов - 88.55).
Наши собственные исследования были проведены в среднегорье Гималаев весной 2009 года и были посвящены влиянию на липопротеидный профиль сыворотки крови комплексного воздействия условий, близких к горноклиматическому лечению, применяемую на курортах бывшего СССР [14, 15, 16]: сочетание высотной гипоксии с регулярной физической нагрузкой (треккинг), к которым мы добавили выполнение упражнений адаптированной тибетской йоги туммо [4].
Всего обследовано 16 здоровых человек (8 мужчин и 8 женщин) в возрасте от 19 до 50 лет, которые с 27.04 по 08.05.2009 находились в среднегорье (2000-3000 м, долина Куллу, Гималаи) и ежедневно выполняли умеренные физические нагрузки (треккинг в среднегорье), а также подвергались холодовым испытаниям на фоне выполнения упражнений для повышения теплопродукции на основе тибетской йоги туммо. Заборы проб крови осуществлялись утром натощак из локтевой вены в 1-ый и 10-ый дни пребывания в условиях среднегорья (Гималаи) на высоте1500 мв лаборатории селения Патликуль (штат Химачал Прадеш, Индия), и на 5-ый день – на высоте3000 мв ущелье Дунди (там же). В лаборатории селения Патликуль проводилось центрифугирование и отбор плазмы для последующего определения липидного профиля на полуавтоматическом биохимическом анализаторе Erba Chem-5 Plus v.2 закрытого типа фотометрическим методом.
Для доказательства достоверности найденных изменений липидного профиля мы применили непараметрический парный критерий Вилкоксона для связанных выборок, поскольку законы распределения изучаемых случайных величин априори неизвестны [20]. Тогда при уровне значимости α = 0.05 (вероятность ошибки первого рода) доказана достоверность следующих изменений липидного профиля между 1-ым и 10-ым днем пребывания в среднегорье на фоне регулярных физических нагрузок:
1. Снижение уровня общего холестерина.
2. Возрастание уровня холестерина в составе липопротеидов высокой плотности.
3. Снижение уровня холестерина в составе липопротеидов низкой плотности.
4. Неизменность уровня холестерина в составе липопротеидов очень низкой плотности.
5. Неизменность уровня триглицеридов.
6. Снижение индекса атерогенности.
Однако в целях единообразия представления статистических оценок для последующего сравнения скоростей изменения липидного профиля мы вынуждены и в нашем случае использовать точечные оценки выборочного среднего арифметического и среднеквадратического отклонения, считая априори, что найденные нами численные значения могут быть описаны параметрами нормального (гауссовского) распределения (X±s(m)). Хотя для нашей выборки (n = 16) найти адекватный закон распределения случайной величины не представляется возможным [20, 21]:
Таблица 4
Изменения липидного профиля на 1, 5 и 10 дни пребывания в среднегорье Гималаев практически здоровых людей (n = 16) в условиях умеренной физической нагрузки и холодовых испытаний (тибетская йога туммо)
|
Показатель |
Содержание в крови |
||
|
на 1 день |
на 5 день |
на 10 день |
|
|
1 |
2 |
3 |
4 |
|
Общий холестерин (ХС), мг/дл |
192.1±27.7(6.9) |
177.4±20.3(7.17) |
173.6±18.7(4.7) |
|
Холестерин ЛПВП, мг/дл |
34.2±5.6(1.4) |
38.25±3.2 (1.15) |
40.8±5.0(1.45) |
|
Холестерин ЛПНП, мг/дл |
132.4±32.4(8.1) |
120.1±12.9(4.55) |
114.4±14.3(3.6) |
|
Холестерин ЛПОНП, мг/дл |
20.6±7.7(1.9) |
19±7.6(2.7) |
18.4±5.4(1.35) |
|
Триглицериды (ТГ), мг/дл |
101.1±40.2(10) |
96.25±37.2(13.2) |
92.4±26.9(6.7) |
|
Индекс атерогенности (ИА), отн.ед. |
4.7±1.1(0.26) |
3.65±0.41(0.14) |
3.37±0.62(0.15) |
Замечание. В таблицах 1, 2, 3 и 4 численные значения липидного профиля крови представлены в виде (X±s(m)), где X – среднее арифметическое, s – выборочное среднеквадратическое отклонение, m=s/√n – стандартная ошибка среднего. Однако для решения задачи сравнения скоростей изменения липидов нам потребуется только численные значения средних арифметических X, поэтому выборочное среднеквадратическое отклонение s и стандартная ошибка среднего m в дальнейшем использоваться не будут.
Математическая модель изменения липидов сыворотки крови
В работах [1-3] описаны антиатерогенные изменения липопротеидов сыворотки крови здоровых людей при подъеме на высоты до 4000 м. Там же доказано, что процесс изменения количества липидов крови на ограниченном временном интервале (от нескольких часов до нескольких недель) вполне адекватно может быть описан известным экспоненциальным выражением, исходя из упрощенной однокомпартментной модели изменения содержания липидов в крови с кинетикой 1-ого порядка [22, 23, 24]:
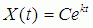
(1)
где X – количество липидов, t – время, k и С – коэффициенты, численные значения которых могут быть вычислены методом наименьших квадратов (далее, МНК). Найденная модель рассматривалась как довод в пользу правомерности результатов, анонсированных К.С.Тринчером о термогенных функциях легких, субстратом которых выступают липиды [2, 3]. Согласно К.С.Тринчеру [5] гипоксемический сигнал, донесенный кровью к легким, вызывает химическую теплопродукцию в легких, независимо от того, какова была причина, вызвавшая гипоксемические сдвиги в крови.
Сравнение скоростей изменения липидов сыворотки крови
Применив МНК, можно найти коэффициенты k и С для экспоненциальной модели (1), которая будет описывать изменения липидов в крови на ограниченном временном интервале (до 30 дней).
Тогда численные данные об усредненном снижении уровня общего холестерина, представленными в таблицах 1, 2, 3 и 4, будут достаточно адекватно, с учетом указанных временных интервалов (от 10 до 30 дней), аппроксимированы аналитическими выражениями:
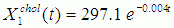
(2)
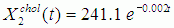
(3)
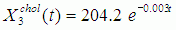
(4)
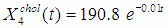
(5)
где X1,2,3,4chol – содержание общего холестерина в крови (нижний индекс показывает номер таблицы, из которой извлечены численные данные об уровне холестерина), t – время.
C целью сравнения скоростей изменения запишем выражения для первых производных по времени:
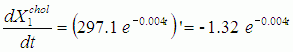
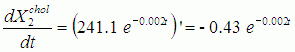
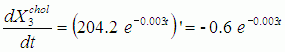

Поскольку сравнение необходимо выполнить на равном временном интервале, то выберем максимальную продолжительность горноклиматического воздействия в рассматриваемой выборке исследований, равную 30 дням. Тогда вычислив определенные интегралы для первых производных от найденных аппроксимирующих функций (2-5) с пределами интегрирования от 0 до 29, и возведя результаты вычислений в квадрат, мы решим задачу сравнения скоростей изменения аппроксимирующих экспонент в пространстве L2 (в квадрате интегрируемых функций) [25]. Выполнив интегрирование и проведя вычисления, находим:
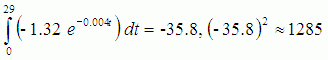
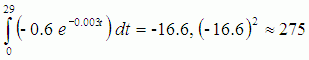
(6)
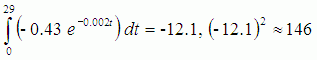
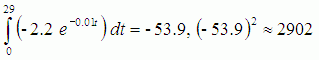
Содержание выражений (6) является доказательством того, что сочетание высотной гипоксии, умеренной физической нагрузки и регулярных холодовых воздействий (тибетская йога туммо для повышения холодоустойчивости – X4chol) дает наибольшую скорость снижения уровня общего холестерина, которая значительно превосходит снижение общего холестерина на фоне только высотной гипоксии (X1chol) и адаптации к гипобарической гипоксии (X2chol). Сочетание высотной гипоксии и умеренной физической нагрузки на фоне санаторно-курортного лечения (X3chol) уже значительно повышает скорость снижения общего холестерина, что нашло далее свое максимальное значение при дополнительном выполнении испытуемыми специальных упражнений на повышение холодоустойчивости (тибетская йога туммо) – X4chol.
Аналогичная последовательность вычислительных операций была применена для сравнения скоростей возрастания ЛПВП и ЛПНП для численных данных, представленных в таблицах 24. Тогда аппроксимирующие экспоненциальные выражения, найденные применением МНК для численных значений липидного профиля, сведенных в таблицах 14, а также вычисленные с их использованием численные значения квадратов определенных интегралов от их первых производных, сведены в таблице 5.
Таблица 5
Сводная таблица экспоненциальных моделей вида Cekt для изменений общего холестерина, ЛПВП и ЛПНП (столбцы 2, 4, 6) и вычисленные с их помощью численные значения квадратов определенных интегралов от их первых производных по времени с пределами интегрирования от 0 до 29 (суток) (столбцы 3, 5, 7).
|
№№ таблицы |
Общий холестерин |
ЛПВП |
ЛПНП |
|||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
1 |
297.1·e-0.004t |
1285 |
|
|
|
|
|
2 |
241.1·e-0.002t |
146 |
37.5·e0.0045t |
27.1 |
161·e-0.001t |
24.3 |
|
3 |
204.2·e-0.003t |
275 |
49.4·e0.003t |
17 |
142.8·e-0.005t |
344 |
|
4 |
190.8·e-0.001t |
2902 |
34.3·e0.02t |
702 |
131.8·e-0.016t |
2480 |
Замечание: Мы проводили оценку скоростей изменения только антиатерогенных (ЛПВП) и проатерогенных (общий холестерин и ЛПНП) фракций липидного состава сыворотки крови. Изменения ЛПОНП и триглицеридов в наших исследованиях оказались незначимыми, поэтому по этим фракциям липидного профиля сравнений не проводили.
Содержание таблицы 5 является доказательством того, что сочетание высотной гипоксии, умеренной физической нагрузки и регулярных холодовых воздействий (тибетская йога туммо для повышения холодоустойчивости – строка 4 ) дает наибольшие скорости снижения общего холестерина, повышения уровня липопротеинов высокой плотности (ЛПВП) и снижения уровня липопротеидов низкой плотности (ЛПНП), которые значительно превосходит изменения липидного профиля на фоне только высотной гипоксии (строка 2) и адаптации к гипобарической гипоксии (строка 3).
Известно, что атерогенные сдвиги липидного профиля крови и липидные пятна на внутренней стенке артерий возникают задолго до клинических симптомов ишемии (начиная с 10-летнего возраста), что делает профилактику дислипидопротеидемий неотъемлемой частью эффективного лечения и реабилитации атеросклероза [26]. Немедикаментозное устранение приобретенных дислипидопротеидемий как одного из главных факторов риска атеросклеротических изменений интимы артерий у здоровых людей составляет заявку на дальнейшие исследования найденных нами методик сочетанной гипокситерапии с целью повышения эффективности горноклиматического лечения кардиологических больных в рамках восстановительной медицины.
Выводы:
1. Найдено новое применение известного вычислительного алгоритма, которое позволяет сравнить скорости изменения во времени липидных фракций крови у здоровых и больных людей в различных условиях.
2. Применением нового вычислительного алгоритма доказано, что наибольшая скорость антиатерогенных изменений липидного профиля крови (снижение общего холестерина и ЛПНП, повышение ЛПВП) характерна для сочетания высотной гипоксии, умеренных физических нагрузок и выполнения специальных упражнений для повышения холодоустойчивости (тибетская йога туммо).
Благодарности:
Автор выражает глубокую благодарность генеральному директору киностудии исторического фильма «Фараон» Ирине Владимировне Архиповой, организатору и вдохновителю международных научно-исследовательских экспедиций в Гималаи в рамках ее авторского проекта «В поисках утраченных знаний» (с), направленного на поддержку отечественной науки.
Литература:
1. Минвалеев Р.С., Иванов А.И. К теории управления организмом человека: Сообщение 6: Тибетская йога Туммо // VIII Международная конференция «Современные технологии восстановительной медицины» 10-15 мая 2005 – Сочи: 2005 – с. 413-416.
2. Минвалеев Р.С., Иванов А.И. К теории управления организмом человека: Сообщение 7: Управляемое снижение атерогенных липидов в условиях высокогорья // X Международная конференция «Профессиональное долголетие и качество жизни». 24–26 сентября 2007. Труды конференции. – М.: 2007. – с. 131132.
3. Иванов А.И., Савельев Е.В. Математическая модель термогенной функции легких в условиях низких температур. Термодинамический подход. // Спортивна медицина (Украина), 2008, №1, с. 170-173.
4. Минвалеев Р.С. Физика и физиология тибетской йоги туммо // Химия и жизнь: XXI век, 2008, №12. - с.28-34.
5. Тринчер К.С. Теплообразовательная функция и щелочность реакции легочной ткани. М.: Издательство АН СССР, 1960.
6. de Mendoza S., Nucete H., Ineichen E., et al. Lipids and lipoproteins in subjects at 1,000 and 3,500 meteraltitudes// Arch Environ Health, 1979, Vol. 34, №5: – p. 308-311.
7. Férézou J., Richalet J.P., Coste T., Rathat C. Changes in plasma lipids and lipoprotein cholesterol during a high altitude mountaineering expedition (4800 m) // Eur J Appl Physiol Occup Physiol, 1988; Vol.57, №6 – p.740-745.
8. Young P.M., Rose M.S., Sutton J.R., et al. Operation Everest II: plasma lipid and hormonal responses during a simulated ascent of Mt. Everest // J Appl Physiol, 1989 Vol. 66, №3. – p. 1430-1435.
9. Férézou J., Richalet J.P., Sérougne C., et al. Reduction of postprandial lipemia after acute exposure to high altitude hypoxia // Int J Sports Med, 1993, Vol.14, №2. – p.78-85.
10. Domínguez Coello S., Cabrera De León A., Bosa Ojeda F. et al. High density lipoprotein cholesterol increases with living altitude // Int J Epidemiol, 2000, Vol.29, №1 – p. 65-70.
11.Schobersberger W., Schmid P., Lechleitner M. et al. Austrian Moderate Altitude Study 2000 (AMAS 2000). The effects of moderate altitude (1,700 m) on cardiovascular and metabolic variables in patients with metabolic syndrome // Eur J Appl Physiol, 2003 Vol.88, №6. – р. 506-514.
12. Temte J.L. Elevation of serum cholesterol at high altitude and its relationship to hematocrit // Wilderness Environ Med, 1996, Vol.7, № 3. – p. 216-224
13. Rühli F.J., Henneberg M., Schär D.J. et al. Determinants of inter-individual cholesterol level variation in an unbiased young male sample // Swiss Med Wkly, 2008, № 138 – p.286–291.
14. Топурия Д.И. Влияние комплексного санаторно-курортного лечения в Кисловодске на липидный обмен у больных хронической ишемической болезнью сердца с постинфарктным кардиосклерозом // Вопросы курортологии, 1975; №3 – с. 247-250.
15. Дудукало Д.П., Рыжук В.В., Ликов А.Ф., Школенко Р.Л. Опыт профилактики ишемической болезни сердца по некоторым факторам риска на пятигорском курорте // Терапевтический архив, 1987, №7. – с.89-91.
16. Миррахимов М.М., Айтбаев К.А., Мураталиев Т.М., Ким И.М. Исследование возможности коррекции атерогенных дислипопротеидемий горноклиматическим лечением // Кардиология, 1991; №3 – с.8-11.
17. Алешин И.А., Тиньков А.Н., Коц Я.И., Твердохлиб В.П. Опыт лечения больных сердечно-сосудистыми заболеваниями методом адаптации к периодической барокамерной гипоксии // Терапевтический архив, 1997, №1. – с.54-58.
18. Тиньков А.Н., Алешин И.А., Коц Я.И. и др.Динамика липидного спектра сыворотки крови у больных ишемической болезнью сердца под воздействием адаптации к периодической барокамерной гипоксии // Кардиология, 1999, № 1. – с. 31-33.
19. Гмурман В.Е. Теория вероятностей и математическая статистика. М.: Высшая школа, 2001. – 479 с., ил.
20. Орлов А.И. Прикладная статистика. Учебник. – М.: Экзамен, 2006. – 671 с.
21. Платонов А.Е. Статистический анализ в медицине и биологии: задачи, терминология, логика, компьютерные методы. – М.: Издательство РАМН, 2000. – 52 с.
22. Eaton R. P., Berman M., Steinberg D. Kinetic Studies of Plasma Free Fatty Acid and Triglyceride Metabolism in Man // J Clin Invest., 1969, Vol. 48, №8. – p. 1560-1579.
23. Shames D.M., Frank A., Steinberg D., Berman M. Transport of plasma free fatty acids and triglycerides in man: a theoretical analysis // J Clin Invest., 1970, Vol. 49, №12. – p. 2298-2314.
24. Atmeh R.F. Metabolism of apolipoproteins A-I and A-II in human high-density lipoprotein: a mathematical approach for analysis of their specific activity decay curves // Biochem Med Metab Biol., 1987, Vol. 38, №3. – p. 317-330.
25. Натансон И.П. Теория функций вещественной переменной. М.: Главная редакция физико-математической литературы издательства «Наука», 1974. – 480 с., ил.
26. Превентивная кардиология: Руководство/ А.В. Виноградов, А.Н. Климов, А.И. Клиорин и др.; под ред. Г.И. Косицкого. – М.: Медицина, 1987. – 512 с.: ил.
Файлы для скачивания:
